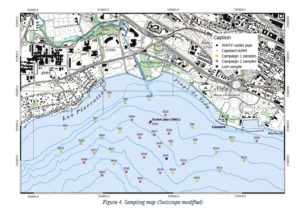
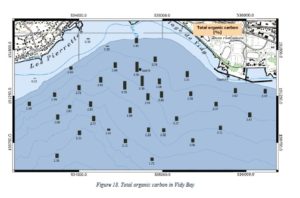
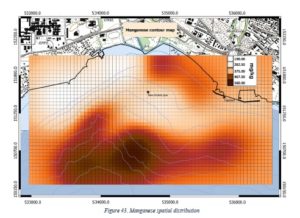
Au cours des 150 dernières années, la plupart des cours d’eau de Suisse ont été canalisés et de nombreux sites naturels ont disparus.
En effet, si nous avons toujours eu besoin d’eau pour vivre, cette dernière peut également présenter un danger lors des inondations. Pour cette raison, mais aussi pour créer de l’énergie ou pour construire, les populations ont cherché à modifier le tracé naturel des cours d’eau. De nombreuses rivières ont ainsi été canalisées ou mises sous tuyau.
Cette modification du tracé des rivières n’a pas été sans conséquences sur l’écologie aquatique. En effet, les cours d’eau qui étaient des mosaïques d’habitats (zones rapides, calmes, gravillons, sédiments fins, etc…) sont devenus des canaux longitudinaux monotones.
Par exemple des poissons comme la truite, qui ont besoin d’un lit de gravier pour pondre, peuvent difficilement se reproduire dans un canal. De même les larves d’insectes, qui se cachent dans les fonds de rivière, ne réussissent pas à s’implanter dans ce même canal.
En 1998, la sonnette d’alarme était tirée. Plusieurs indicateurs montraient que les populations de poissons étaient menacées en Suisse. Les relevés indiquaient une diminution des prises de truites allant jusqu’à 50 % depuis les années 1980, l’habitat dégradé et la pollution étant des facteurs causals robustes.
Entre 1997 et 2008, l’état de 65’000 km du réseau hydrologique suisse a été évalué par l’Office fédérale de l’environnement. La Figure 1 présente l’état de la situation en 2009. Les graphiques montrent que plus de 75% du réseau d’eau en zone urbaine est très affecté, artificiel ou souterrain. Difficile pour la biologie de faire sa place.
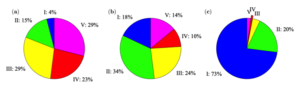
Figure 1: Etat hydromorphologique des rivières en Suisse par zones en 2009 : (a) urbaine, (b) agricole et (c) autre. I = naturelle (bleu), II = peu affectée (vert), III = très affecté (jaune), IV = artificiel (rouge) et V = souterraine (magenta). Source : (Office fédéral de l’environnement 2009).
Sur la base de ce constat et suite à la modification de la Loi sur la protection des eaux en 2011, le gouvernement suisse a prévu la restauration de 4’000 km de rivière d’ici 2090. La renaturation implique le rétablissement des fonctions naturelles et la restauration de l’habitat pour obtenir une faune et une flore diversifiées. 307 km de rivières avaient déjà été renaturés en 2014.
Mais la restauration est un travail colossal et très coûteux.
De plus, rendre à la rivière sa place implique de prendre du terrain sur le milieu urbain, ou sur les terres agricoles, ce qui n’est pas toujours très simple.
S’y ajoute un autre problème, mis en évidence récemment par des chercheurs allemands dans leur article “Poison au paradis”. Ces auteurs montrent que le succès des renaturations n’est peut-être pas toujours au rendez-vous, ceci au vu de la pollution chimique de l’eau, et surtout des sédiments, dans les zones renaturées.
En effet, les activités humaines dans les bassins versants des cours d’eau génèrent une pollution diffuse dans la rivière. Le ruissellement sur les routes en milieu urbain entraîne des métaux issus de l’abrasion des véhicules, du mobilier urbain ou des toitures, vers les grilles d’égouts, puis vers les cours d’eau. Il entraîne également des pesticides utilisés dans les jardins, et bien d’autres polluants. En zone agricole, des pesticides, toujours, sont également emmenés jusque dans les rivières lors des pluies.
Or cette pollution est rarement mesurée avant une renaturation. Les évaluations des corrections des cours d’eau tendent à se concentrer sur les modifications de l’écomorphologie, soit du lit du cours d’eau.
Les chercheurs se sont donc penchés sur le cas de la rivière Nidda, en Allemagne. Cette rivière a un bassin versant de 2000 km2, avec une importante pression agricole et industrielle. Ils ont comparé la toxicité de l’eau et des sédiments prélevés dans une zone renaturée, avec celle d’échantillons pris dans une zone peu impactée en amont de la rivière. Ils ont ainsi montré, en laboratoire, que les organismes biologiques étaient fortement impactés par les échantillons provenant de la zone renaturée, alors qu’ils ne l’étaient que peu par ceux provenant de la zone en amont.
Pour les auteurs allemands, la pollution est un facteur de stress persistant pour le cours d’eau, ce qui peut limiter la récupération de la biologie dans les zones renaturées.
Si on veut donner une chance aux écosystèmes des rivières, il semble donc important de re-créer des habitats, mais également d’assainir le bassin versant. Cela passe donc par une réflexion sur les mesures qui peuvent être prises pour limiter les rejets vers les eaux
Sinon, il y a de fortes chances que la biologie ne se réapproprie pas des zones qui, bien que paraissant naturelles, restent toxiques.
Références:
Brettschneider, DJ, Misovic A, Schulte-Oehlmann U, Oetken M & Oehlmann J. 2019. Poison in paradise: increase of toxic effects in restored sections of two rivers jeopardizes the success of hydromorphological restoration measures. Environmental Sciences Europe. 31:36.
Office fédéral de l’environnement (OFEV). 2009. Ecomorphologie des cours d’eau suisses: Etat du lit des berges et des rives. Résultats des relevés écomorphologiques (avril 2009). Confédéderation suisse, Berne.